Índice del artículo
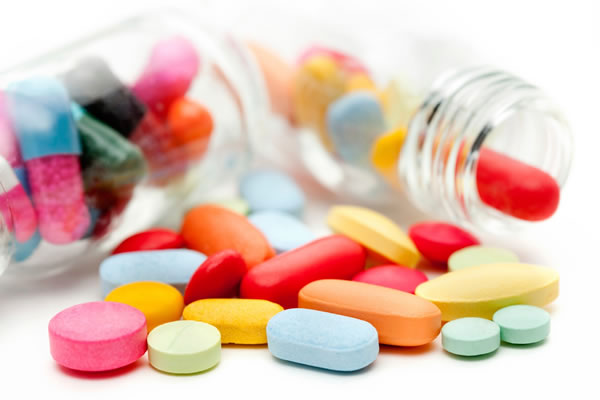
Comenzaremos con la Validación de Proceso (fig.1), haciendo un comparativo actual y tradicional y los requerimientos normativos (fig. 2)
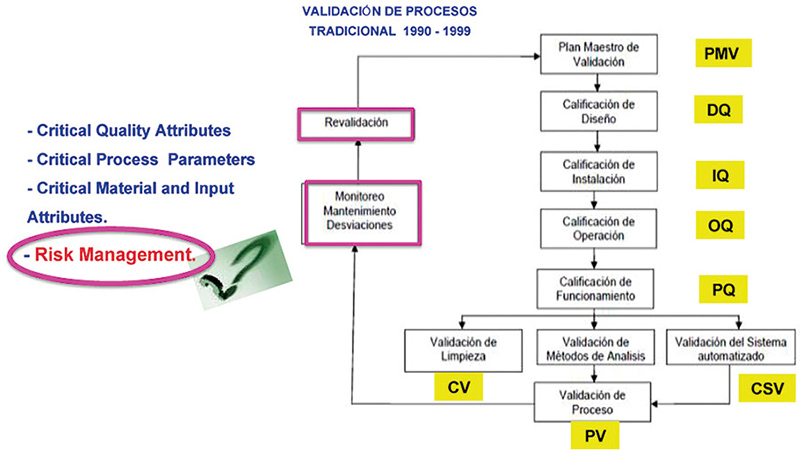
Figura 1
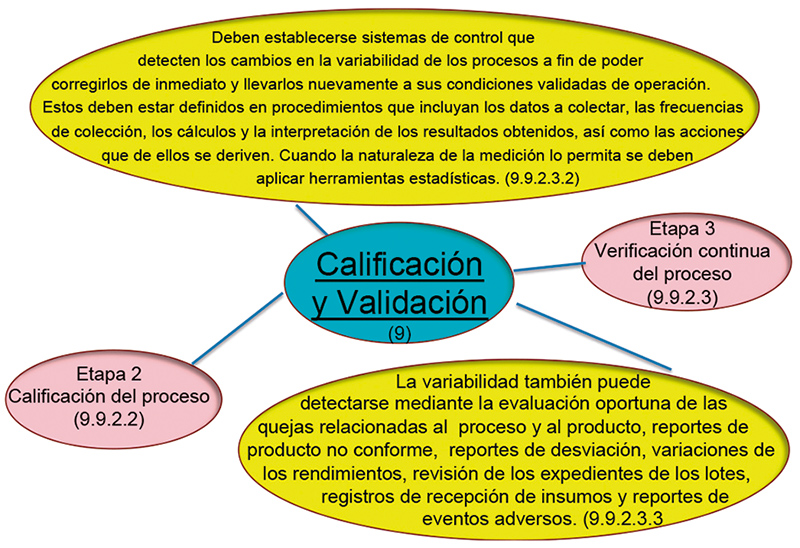
Figura 2
Tenemos complementos interesantes ahora, los cuales son: gestión de riesgos, identificación de CQA, CPP y CMAIA, uso de estadística para generar sistemas de control que detecten los cambios en la variabilidad de los procesos (Six Sigma) y la forma de afectación por la variabilidad debida a los reportes colectados por el sistema de calidad (9.9.2.3.3), siendo el reto que lo enfoquemos a la oportunidad de generar valor al negocio a través del cumplimiento regulatorio. (fig.3).

Figura 3
Por lo que, con estas armonizaciones internacionales FDA – EMA – OMS – NOM-059-SSA1-2015, serie ISO, principalmente, necesitamos cambiar la forma de pensamiento, romper paradigmas, pensar fuera de la caja, si todos los caminos nos llevan a Roma, esto indica que todo nos lleva al concepto Lean Validation, el mantenimiento del estado validado en los tres lotes de validación en todo el ciclo de vida del producto de los lotes comerciales, y correlacionarlo a la estrategia de control a desarrollar e implementar en el proceso de validación. (fig. 4 y 5).

Figura 4
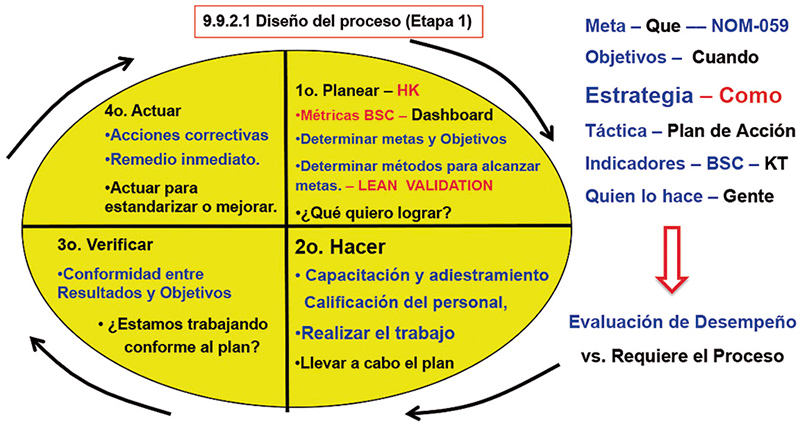
Figura 5