Agencias. Hangzhou Sciwind Biosciences anunció una colaboración estratégica de comercialización con Pfizer China para la inyección de Ecnoglutida (Ecnoglutida), un agonista del receptor GLP-1 de nueva generación con sesgo de AMPc.
En virtud del acuerdo, Pfizer obtendrá los derechos exclusivos de comercialización del producto en China continental, lo que marca un primer paso importante para impulsar la estrategia global de Pfizer en el campo metabólico en China. Sciwind Biosciences seguirá siendo el titular de la autorización de comercialización y será responsable de la investigación y el desarrollo, el registro, la fabricación y el suministro del producto. Según los términos del acuerdo, Sciwind Biosciences puede recibir hasta 495 mdd en pagos iniciales, regulatorios y por hitos de ventas.
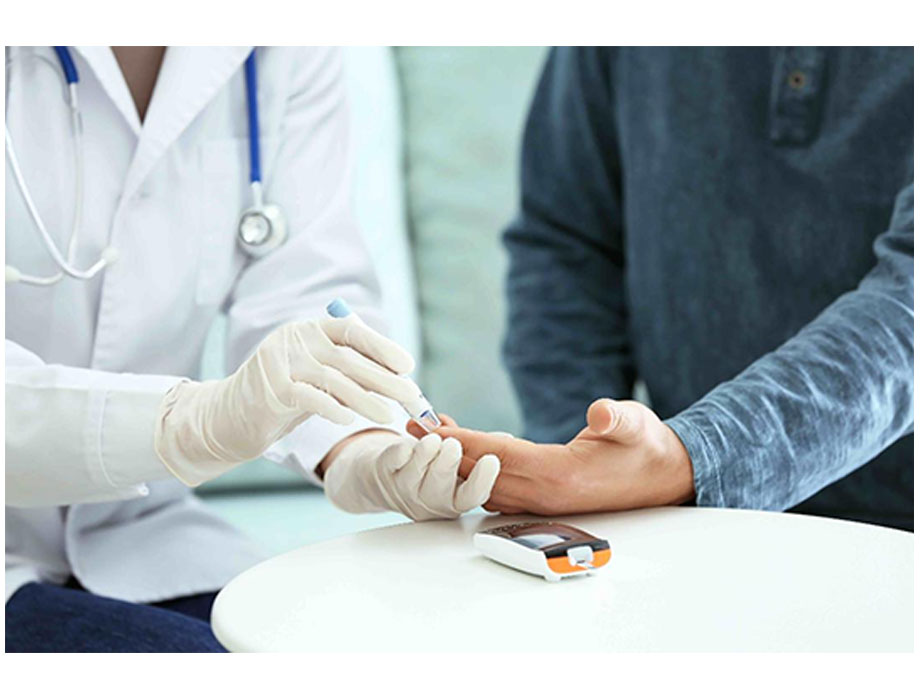
Ecnoglutide fue desarrollado independientemente por Sciwind Biosciences y es un agonista del receptor GLP - 1 sesgado por cAMP de nueva generación. Está diseñado para proporcionar opciones de tratamiento más precisas para pacientes con diabetes tipo 2 y necesidades de control de peso a largo plazo Con su mecanismo de señalización sesgado único, la inyección de Ecnoglutide ha demostrado un sólido perfil de eficacia y seguridad en múltiples estudios clínicos, logrando en pacientes chinos una pérdida de peso ajustada a placebo del 15.1%, el 92.8% de los pacientes logrando una pérdida de peso clínicamente significativa y más del 80% de los pacientes logrando niveles de HbA 1c por debajo del 7%. La inyección de Ecnoglutide fue aprobada por la Administración Nacional de Productos Médicos de China (NMPA) en enero de 2026 para el tratamiento de la diabetes tipo 2 en adultos, y su solicitud de autorización de comercialización para el control de peso crónico en adultos ha sido aceptada por la NMPA de China.
Pan Hai, fundador y director ejecutivo de Sciwind Bioscience, declaró: “Motivados por nuestra misión de transformar la vida con la ciencia, Sciwind Biosciences se dedica a abordar las necesidades urgentes de salud en el ámbito del control de peso. Creemos firmemente que Pfizer, como compañía farmacéutica líder a nivel mundial, posee un profundo conocimiento y una sólida capacidad de ejecución en el mercado chino. A través de esta colaboración estratégica con Pfizer China, esperamos integrar plenamente los innovadores logros científicos de Sciwind Biosciences con las excelentes capacidades de comercialización de Pfizer China para acelerar la comercialización de Ecnoglutida. Considerando el «Año del Control de Peso» como una oportunidad clave, nos proponemos colaborar para ofrecer opciones de tratamiento más diversas y de mayor calidad para pacientes con obesidad y enfermedades metabólicas en China”.
Hoy también publicamos las siguientes notas y más...
Hasta 10 millones de personas en México viven con una enfermedad rara