Agencias. Recientemente, la FDA aprobó el uso de gotas mióticas para tratar la presbicia, ya que ayudan a ablandar el cristalino y a restaurar su flexibilidad.
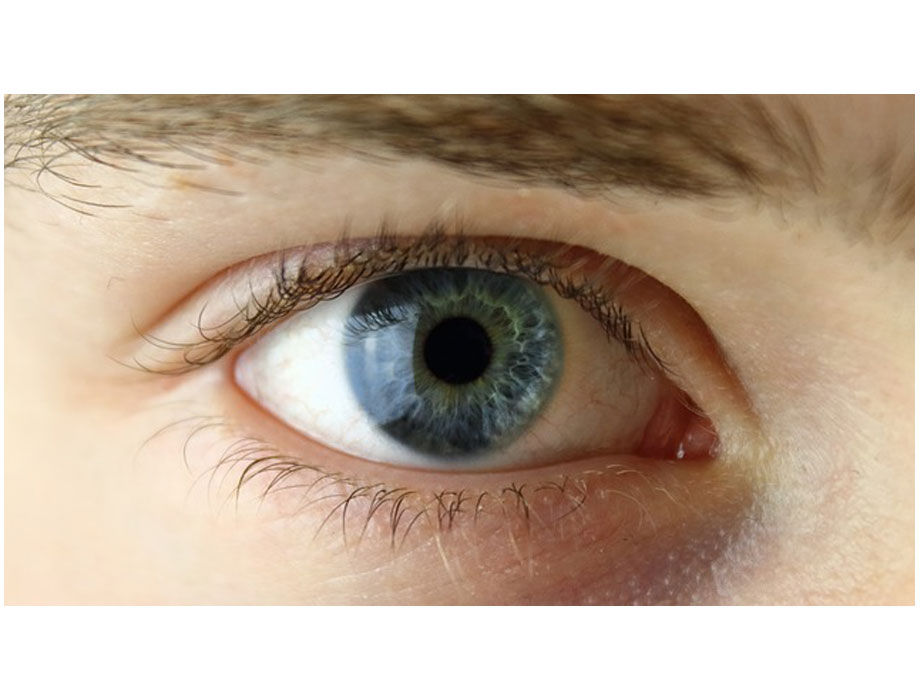
Al respecto, la Academia Americana de Oftalmología explicó que estas gotas cambian el tamaño de la pupila, debido a que crean un “efecto de agujero del tamaño de la punta de un alfiler” y maximizan el enfoque de cerca y de lejos.
Christopher Starr, oftalmólogo de Weill Cornell Medicine en la ciudad de Nueva York, explicó: “La importancia de esta aprobación de la FDA es fundamental, ya que hay aproximadamente 2,000 millones de personas en todo el mundo con presbicia. Las gafas, los lentes de contacto y la cirugía son tratamientos tradicionales, pero por diversas razones, no funcionan bien para todos los pacientes. Tener la opción de un tratamiento novedoso en forma de gotas oftálmicas para la presbicia es una adición bienvenida a nuestra lucha contra esta condición universal de visión cercana relacionada con la edad, que afecta esencialmente a todas las personas mayores de 40 años”.
De acuerdo con el experto, estas gotas ayudan a que el ojo enfoque mejor los objetos que se encuentran cerca, debido a que ablandan el cristalino; aunque no pueden restaurar por completo la visión de cerca, sí son de gran ayuda, al menos, durante los próximos 10 años.
La Academia Americana de Oftalmología indicó que algunos estudios sugieren que las gotas mióticas comienzan a actuar en unos 30 minutos y suelen tener una duración de siete horas.
Por otro lado, la FDA también aprobó la utilización de Yuvezzi, una terapia desarrollada por la compañía biotecnológica Tenpoint Therapeutics, que acaba de recibir la aprobación para su venta y es el primer colirio de doble acción que restaura la visión de cerca hasta por 10 horas.
Hoy también publicamos las siguientes notas y más...
Pfizer nombra a Ricardo Castellan como su nuevo presidente para Brasil
OMS llama a ayudar a millones de personas en entornos de crisis y emergencias de salud