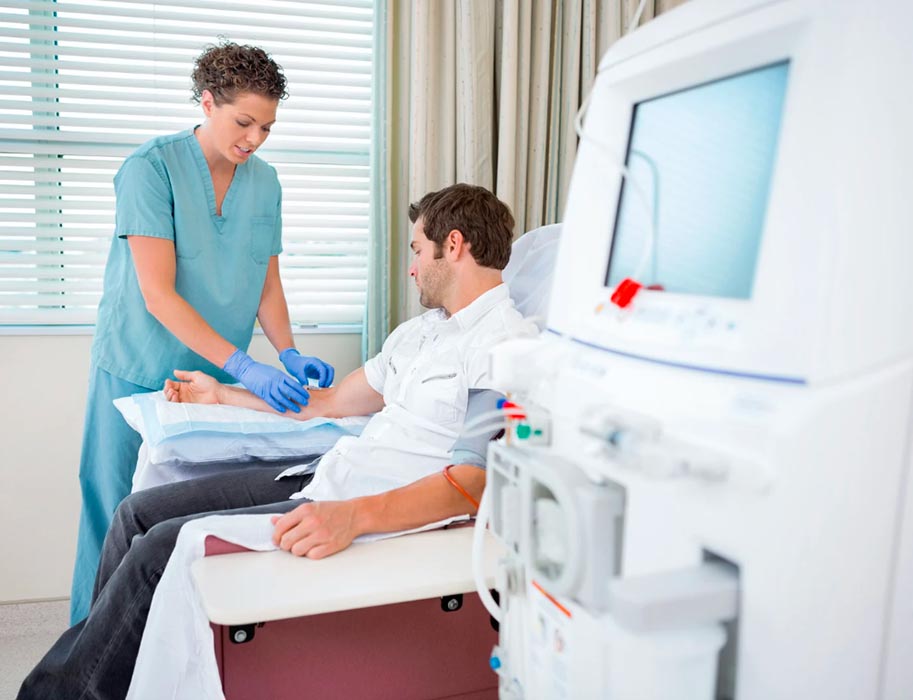
Comunicado. El cáncer de vejiga del cual el 90% es cáncer urotelial es una enfermedad silenciosa que, sin detección oportuna, puede extenderse al sistema urinario y convertirse en un grave riesgo para la salud. En México, es la 14ª causa de muerte, lo que resalta la urgencia de terapias más efectivas. Afortunadamente, los avances médicos en el cáncer urotelial están revolucionando su manejo, ofreciendo opciones más completas y mejorando la calidad de vida de los pacientes.
En México, el sistema de Salud Pública ha dado un giro innovador en el manejo del cáncer urotelial, mejorando el acceso a servicios médicos especializados. Actualmente, las terapias no solo son más efectivas, sino también menos invasivas que los procedimientos médicos tradicionales. Esta evolución no sólo alivia la presión sobre el sistema de salud, sino que también brinda a los pacientes la oportunidad de vivir con mayor bienestar y autonomía, abriendo nuevas puertas hacia una vida más plena de todas las personas que conviven con el cáncer de vejiga.
Un claro ejemplo de este avance es avelumab, una terapia que amplía las opciones de inmunoterapia para personas con cáncer de vejiga que han respondido favorablemente a la quimioterapia. Esta innovación ofrece un nuevo horizonte en la atención de salud pública. Como explica el médico oncólogo José Manuel Ruiz Morales, “esta terapia podría aumentar la supervivencia alrededor de 30 meses, es decir, dos veces más que las acciones tradicionales de quimioterapia sin terapia de mantenimiento”.
Como algunas inmunoterapias, avelumab devuelve al cuerpo la capacidad de reconocer al cáncer y se enfoca específicamente en el tumor, minimizando el daño a las células sanas. "Su incorporación en el proceso fortalece la respuesta inmune, permitiendo al cuerpo combatir el cáncer de forma más efectiva y con menos ciclos de terapia. Así, se convierte en una opción más suave y potente frente a los métodos tradicionales", añade Ruiz Morales.
El cáncer de vejiga está estrechamente vinculado a varios factores de riesgo, como el tabaquismo, la exposición a productos químicos industriales, infecciones crónicas del tracto urinario y antecedentes genéticos. Según el oncólogo, “el tabaquismo es el mayor factor de riesgo para el cáncer urotelial, ya que las toxinas del humo dañan las células de la vejiga. De hecho, los fumadores tienen tres veces más probabilidades de desarrollar esta afección que los no fumadores”.
Hoy también publicamos las siguientes notas y más...
En México, 40% de la población nunca se ha realizado pruebas de infecciones de transmisión sexual
FDA acepta solicitud del tratamiento de Teva para prevenir la migraña episódica pediátrica