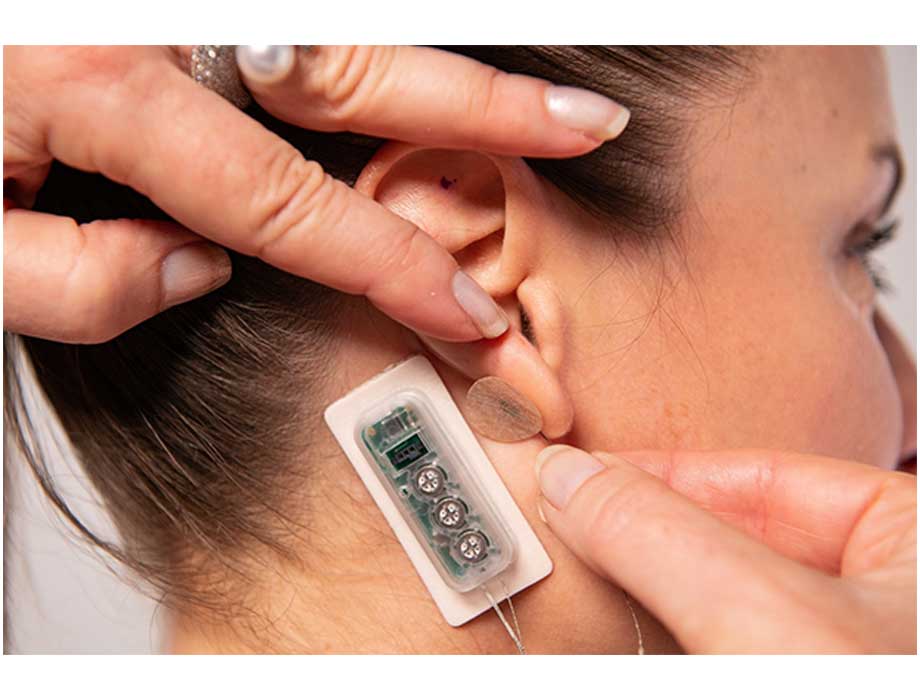
Comunicado. DyAnsy dio a conocer que Dans First Relief, un dispositivo PENS (neuroestimulación eléctrica percutánea), ha sido aprobado por la FDA para múltiples tratamientos de hasta 56 días, para el alivio sintomático de enfermedades crónicas, dolor intratable de la neuropatía periférica diabética.
El dispositivo portátil colocado en la oreja administra pulsos continuos de una corriente eléctrica de bajo nivel durante varios días.
“Estamos entusiasmados de tener la aprobación de First Relief por parte de la FDA para que este dispositivo, que ha demostrado ser efectivo, ahora pueda usarse para tratar a pacientes que han estado experimentando dolor relacionado con la neuropatía diabética. First Relief ofrece una opción de tratamiento importante sin drogas ni narcóticos”, dijo Srini Nageshwar, director ejecutivo de DyAnsy.
La aprobación se basó en un estudio que probó First Relief contra un placebo y otro dispositivo aprobado previamente por la FDA. El estudio se realizó en el Jeevak Multispeciality Hospital en Warangal, India, reconocido por el tratamiento de la diabetes. El estudio prospectivo de un solo centro, de tres brazos, aleatorizado, controlado, de asignación paralela, doble ciego, involucró a 63 pacientes de 30 a 74 años.
Los dispositivos se aplicaron cada dos semanas durante 16 semanas. El criterio principal de valoración de la eficacia fue la intensidad del dolor medida a través de la puntuación de la escala analógica visual (VAS) y los criterios de valoración secundarios de la eficacia son el valor del umbral de percepción de la vibración (VPT), el índice de gravedad del insomnio (ISI), la escala general de limitaciones de la neuropatía (ONLS), la escala de calificación de Hamilton para la ansiedad.
El análisis de la puntuación del dolor VAS mostró una reducción significativa en la puntuación del dolor de los pacientes tratados con First Relief desde el comienzo del tratamiento hasta el final. Esta mejora persistió durante los 90 días de seguimiento, lo que sugiere que el tratamiento fue una mejora a largo plazo del dolor neuropático y no una mejora a corto plazo. Las medidas de resultado secundarias (VPT, insomnio, ONLS y HAM) también mostraron mejoras similares en la puntuación del dolor, mostrando una mejora significativa en el sueño y el estado de ánimo a medida que disminuía el dolor neuropático. No se observaron complicaciones ni eventos adversos en ninguno de los sujetos durante el periodo de estudio.
Hoy también publicamos las siguientes notas y más...
FDA advierte sobre medicamentos para disfunción eréctil ocultos en suplementos de hierbas
Vacunación infantil sufre mayor descenso en 30 años: OMS y UNICEF